Factores que influyen en la cloración
Entre los principales factores que influyen en el proceso de desinfección y tratamiento del agua con cloro, figuran los siguientes:
-Naturaleza, concentración y distribución de los organismos que se van a destruir, así como de la concentración y distribución de la sustancia desinfectante y de los productos de su reacción con el agua, así como de las sustancias disueltas o en suspensión presentes en el agua.
-Naturaleza y temperatura del agua objeto del tratamiento.
-Tiempo de contacto entre el cloro y el agua.
-Ph del agua.
Respecto a los anteriores factores, podemos decir, en lo que respecta a los organismos presentes en el agua, que estos pueden ser muy diversos y con unos requerimientos de cloro para su eliminación muy diferentes.
En el proceso de cloración y en la desinfección en general, las variables usualmente más controlables son:
1) La naturaleza y concentración del desinfectante
2) El tiempo de contacto entre el desinfectante y los microorganismos
3) La mezcla, dispersión y grado de agitación del agua.
Para que la cloración resulte eficaz es necesaria una distribución homogénea del cloro en el agua y que la dosis sea adecuada, para obtener un agua tratada inocua. A partir de 0,1 a 0,2 ppm. de cloro libre residual en el agua, ya se percibe sabor, percibiéndose antes cuanto mayor sea la dureza y temperatura del agua. Puede procederse a la decloración o eliminación del cloro en el agua, mediante el empleo de sustancias reductoras, tales como el anhídrido sulfuroso, el hiposu1fito sódico, etc.,. Utilizando cantidades apropiadas de estos productos se puede eliminar la cantidad de cloro deseada. También se puede eliminar el cloro filtrando el agua a través de carbón activo.
Entre las múltiples sustancias que pueden contener las aguas naturales, algunas influyen en gran medida en la eficacia de la cloración. Por ejemplo, en presencia de sustancias orgánicas, la acción desinfectante del cloro es menor. El amoníaco y otros compuestos orgánicos nitrogenados consumen cloro. El hierro y el manganeso reaccionan con el cloro aumentando la demanda de éste, y, una vez oxidados, contribuyen a aumentar la turbiedad del agua.
Las bacterias y virus pueden quedar protegidos de la acción del cloro por los sólidos suspendidos en el agua; de aquí que la eficacia de la cloración se vea aumentada mediante la subsiguiente filtración y una posterior esterilización.
Respecto a la temperatura, la eficacia de cloración aumenta al aumentar aquélla, naturalmente siempre que las demás condiciones permanezcan invariables. A pesar de esto, ocurre que como en el agua a baja temperatura el cloro permanece más tiempo, puede llegar a compensarse la mayor lentitud de la desinfección con la mayor duración del cloro en el agua.
El tiempo de contacto es otro factor importante a tener en cuenta, ya que durante este tiempo tienen lugar las reacciones entre el cloro y el agua y las sustancias en ella presentes. El tiempo de contacto mínimo suficiente para una cloración eficaz es, a su vez, función de la temperatura, pH, concentración y naturaleza de los organismos y sustancias presentes en el agua, así como de la concentración y estado en que se halle el cloro. Como mínimo, el tiempo de contacto deber de ser de diez a quince minutos.
Para que la acción de un desinfectante sea eficaz, hay que mantener una determinada concentración del desinfectante durante un período de tiempo, es decir, la expresión C.t, representaría la concentración del desinfectante final en mg./l. (C) durante el tiempo mínimo de exposición en minutos (t ). La expresión que nos muestra el efecto de la concentración del desinfectante sobre la velocidad de destrucción de bacterias, se expresa más correctamente por Cn . t = Constante.
El exponente n para el cloro varía entre 0.5 y 1.5, dependiendo de la temperatura y del pH
El pH juega un papel de suma importancia y nos detendremos en él cuando tratemos de las reacciones del cloro en el agua. Por ahora diremos que el poder bactericida del cloro es menor para un pH superior a 7, que para otros valores de pH más bajos a éste.
El tiempo de contacto para lograr un determinado grado de desinfección disminuye al aumentar la concentración y tambien como se acaba de indicar, al disminuir el pH. En el gráfico siguiente se observa lo indicado, relacionando el tiempo de contacto necesario para destruir el 90 % de coliformes a diferentes pH.
Reacciones del cloro en el agua
Las reacciones que tienen lugar entre el cloro y el agua, aunque en principio parecen muy simples, no siempre lo son, ya que el agua objeto de la cloración no sólo es H2O, sino que en ella hay diversas sales y materias orgánicas en solución y suspensión. Pero trataremos en principio sólo de las reacciones de equilibrio que tienen lugar al reaccionar el cloro con el agua,que son reacciones de hidrólisis , se originan ácidos hipocloroso y clorhídrico :
CL2 + H2O ↔ CLOH + CLH (1)
El ácido clorhídrico es neutralizado por la alcalinidad del agua y el ácido hipocloroso se ioniza, descomponiéndose en iones hidrógeno e iones hipoclorito:
CLOH ↔ H+ + CLO– (2)
La constante de ionización del anterior equilibrio es:
[ H+] * [CLO–]
———————– = Ki (3)
[ CLOH ]
La constante de ionización K1 varía con la temperatura como se indica en la siguiente tabla:
| Temper. ºC | 0 | 5 | 10 | 15 | 20 | 25 |
| (Moles/l) Ki | 1,5.10-8 | 1,5.10-8 | 2,0.10-8 | 2,2.10-8 | 2,5.10-8 | 2,7.10-8 |
La constante de hidrólisis de la reacción (1) es de tal orden que no existe en el agua una concentración apreciable de CL2 a no ser que la concentración de H+ sea elevada, es decir, que el pH del agua sea bajo, menor de 3, y haya una concentración total de cloruros mayor de 1.000 mg/l.
A las temperaturas ordinarias del agua, la hidrólisis del cloro es prácticamente completa en algunos segundos y la ionización del ácido hipocloroso es una reacción reversible instantánea. El sentido de esta reacción, es fácil ver que se encuentra dirigido por la concentración de iones hidrógeno, es decir del pH. Por tanto, se puede decir que según sea el pH del agua, se obtendrán unos porcentajes diversos de CLOH y CIO– , porcentajes que pueden calcularse mediante la ecuación (3) y la tabla anterior en la que figuran los valores de Ki partiendo de la relación:
[ClOH] [CIO–]
—————————- = 1 ÷ ( 1 + ————-) (4)
[ClOH ] [ClO–] [ClOH]
[CLO–] Ki
Y deduciendo de la ecuación (3) que: ————— = ———-
[CLOH] [H+]
[CLOH] Ki
sustituyendo en (4), resulta : ————————– = 1 ÷ ( 1 + ———-) (5)
[CLOH] + [CLO–] [H+]
Por ejemplo a 20 º C y pH = 7 , el porcentaje de ClOH será según (5) :
1
_______________________ ; de donde CLOH = 80 %
2,5 . 10-8
1+ —————
10-7
Demanda de cloro y Break point
La cantidad de cloro que debe utilizarse para la desinfección del agua, se determina generalmente mediante el método de la demanda de cloro y el de breakpoint.
Al incorporar el cloro al agua, reacciona con las sustancias que ésta contiene, quedando menos cloro en disposición de actuar como desinfectante. Entre estas sustancias destacan el manganeso, hierro, nitritos, sulfhídrico y diferentes materias orgánicas, las cuales, además de consumir cloro, producen compuestos orgánicos clorados que pueden ser la causa de olores y sabores desagradables. Otra sustancia presente, a veces ,en el agua y que reacciona de una forma muy particular con el cloro es el amoníaco. En este caso se forman compuestos denominados cloraminas, las cuales poseen poder desinfectante, aunque en menor grado que el cloro.
Si se continúa añadiendo cloro en exceso, de manera que reaccione con todas las sustancias presentes, llegará un momento en que el cloro sobrante aparecerá como cloro residual libre, que es el que realmente actúa ahora como agente desinfectante.
La demanda de cloro es la diferencia entre la dosis de cloro añadida y el contenido de cloro residual al cabo de un tiempo de contacto suficiente para completar las reacciones antes expuestas.
El control perfecto de la desinfección, se efectúa mediante los correspondientes exámenes bacteriológicos del agua, pero para un control más rápido del contenido en cloro libre y combinado de un agua tratada, se determina la concentración de cloro residual mediante el método del DPD, o bien por yodometría y valoración con tiosulfato sódico; también, en instalaciones importantes suelen emplearse instrumentos automáticos de medida permanente, mediante determinaciones colorimétricas o determinaciones amperométricas.
El cloro presente en el agua tratada que se conoce como «cloro residual», puede presentarse como «cloro residual libre» o como «cloro residual combinado».
El cloro residual libre está constituido esencialmente por el ácido hipocloroso y el ión hipoclorito; y el cloro residual combinado lo forman generalmente las cloraminas.
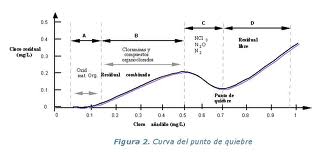
Para que el cloro residual libre esté presente en un agua tratada con cloro después del suficiente tiempo de contacto, es necesario que la cloración se lleve a cabo mediante una dosis lo suficientemente elevada de cloro, hecho conocido como «dosificación con cloro sobrante», «cloración por el punto crítico» o «cloración al breakpoint», con lo cual el cloro oxidará todas las sustancias que estén en disposición de ser oxidadas, se combinará, destruirá y eliminará otras, como por ejemplo las cloraminas , y después de todo esto aún quedará un exceso de cloro libre residual. La dosis de cloro a la cual comienza a aparecer el cloro libre residual es la llamada dosis de breakpoint. Indicaremos ahora, y después ampliaremos, que algunas de las sustancias orgánicas cloradas formadas con el cloro libre son causa de preocupación desde el punto de vista sanitario.
Teóricamente, en un agua totalmente pura, al ir adicionando cloro, la concentración residual medida del mismo sería igual al cloro incorporado. Pero esto no ocurre así en aguas que no son completamente puras, que es el caso general. Entonces, al ir adicionando cloro y después de haberse oxidado las diversas sustancias que ya indicamos y formado las cloraminas, si había presente amoníaco y otros compuestos clorados de adición, si medimos ahora el cloro residual, se observará que éste no corresponde al añadido, sino que es menor, llegando incluso a un punto, en que en lugar de ir aumentando la concentración de cloro residual ésta disminuye. La explicación de este descenso se justifica por el hecho de que una vez formados los diversos derivados orgánicos del cloro y las cloraminas, llegan a destruirse mediante la adición de más cloro, formándose otros compuestos que no suministran cloro residual. Cuando se han destruido estos compuestos clorados, comienza a aparecer el cloro residual libre, ya medida que se añade cloro al agua aumenta la concentración de cloro residual libre, pudiendo subsistir a la vez una pequeña concentración de cloro residual combinado, debido a compuestos que no han sido destruidos totalmente. Se considera que cuando el 85 % ó más del cloro residual del agua está en forma libre, la desinfección se ha realizado al breakpoint.
Cuando se realiza una cloración al breakpoint, no sólo es el CIOH que persiste al terminar las reacciones ( cloro residual libre) el que se utiliza para la desinfección, sino que también se está utilizando, en parte, para la desinfección, el CIOH que existe durante el desarrollo y consecución del breakpoint. Esta disponibilidad temporal de CIOH es función del pH, temperatura y concentración de cloro y amoníaco.
Demanda de cloro
La cantidad de cloro que debe utilizarse para la desinfección del agua, se determina generalmente mediante el método de la demanda de cloro y el de breakpoint.
Al incorporar el cloro al agua, reacciona con las sustancias que ésta contiene, quedando menos cloro en disposición de actuar como desinfectante. Entre estas sustancias destacan el manganeso, hierro, nitritos, sulfhídrico y diferentes materias orgánicas, las cuales, además de consumir cloro, producen compuestos orgánicos clorados que pueden ser la causa de olores y sabores desagradables. Otra sustancia presente, a veces ,en el agua y que reacciona de una forma muy particular con el cloro es el amoníaco. En este caso se forman compuestos denominados cloraminas, las cuales poseen poder desinfectante, aunque en menor grado que el cloro.
Si se continúa añadiendo cloro en exceso, de manera que reaccione con todas las sustancias presentes, llegará un momento en que el cloro sobrante aparecerá como cloro residual libre, que es el que realmente actúa ahora como agente desinfectante.
La demanda de cloro es la diferencia entre la dosis de cloro añadida y el contenido de cloro residual al cabo de un tiempo de contacto suficiente para completar las reacciones antes expuestas.
El control perfecto de la desinfección, se efectúa mediante los correspondientes exámenes bacteriológicos del agua, pero para un control más rápido del contenido en cloro libre y combinado de un agua tratada, se determina la concentración de cloro residual mediante el método del DPD, o bien por yodometría y valoración con tiosulfato sódico; también, en instalaciones importantes suelen emplearse instrumentos automáticos de medida permanente, mediante determinaciones colorimétricas o determinaciones amperométricas.
El cloro presente en el agua tratada que se conoce como «cloro residual», puede presentarse como «cloro residual libre» o como «cloro residual combinado».
El cloro residual libre está constituido esencialmente por el ácido hipocloroso y el ión hipoclorito; y el cloro residual combinado lo forman generalmente las cloraminas.
Para que el cloro residual libre esté presente en un agua tratada con cloro después del suficiente tiempo de contacto, es necesario que la cloración se lleve a cabo mediante una dosis lo suficientemente elevada de cloro, hecho conocido como «dosificación con cloro sobrante», «cloración por el punto crítico» o «cloración al breakpoint», con lo cual el cloro oxidará todas las sustancias que estén en disposición de ser oxidadas, se combinará, destruirá y eliminará otras, como por ejemplo las cloraminas , y después de todo esto aún quedará un exceso de cloro libre residual. La dosis de cloro a la cual comienza a aparecer el cloro libre residual es la llamada dosis de breakpoint. Indicaremos ahora, y después ampliaremos, que algunas de las sustancias orgánicas cloradas formadas con el cloro libre son causa de preocupación desde el punto de vista sanitario.
Cloro residual en la red de distribución
El consumo de cloro en el agua de una red de distribución se debe, por una parte, al consumo del cloro por la propia agua (sustancias presentes en ella y otras condiciones físicas) y por otra, al consumo que se produce en la interfase con las paredes de las conducciones.
En el agua, el consumo depende principalmente de la temperatura y del contenido en materias orgánicas disueltas (COT).
En la interfase con las paredes, el consumo de cloro se produce por la interacción con los productos de corrosión y por los depósitos y biomasa fijada en las paredes.
La disminución del cloro residual en una masa de agua, viene expresada por la ecuación exponencial siguiente:
C(t) = C0.e-kt
C(t) = Concentración de cloro (mg/l.) en el tiempo t.
C0 = Concentración inicial de cloro (mg/l.)
t = Tiempo de reacción.
Es decir, hay una disminución exponencial de cloro residual con el tiempo.
La constante K puede ser calculad por la siguiente ecuación:
K = ln (C0/Ct)
T
Un tiempo de exposición mínimo es necesario para que la concentración de cloro aplicado garantice la desinfección.
En 1908, los investigadores Chick y Watson desarrollaron lo se llamó la ley de Chick . Este principio describe el tiempo y la concentración de desinfectante que se necesita para matar los microbios en el agua , determinaron que al aumentar el tiempo de duración del contacto del desinfectante en el agua, disminuye el número de microbios en esta comprobandose que este producto es importante en la destrucción de microbios potencialmente nocivos.
Para un agua correctamente pretratada, se debe mantener un C.t del orden de 15 (mg.min/.l), por ejemplo 0,5 mg/l. de cloro libre durante 30 minutos, ó 0,25 mg/l. durante 1 hora.
A título de ejemplo comparativo, se muestran valores C.t para diversos desinfectantes:
Cloro = 15 (0,25 mg/l. durante 60 minutos)
Ozono = 1,6 (0,40 mg/l. durante 4 minutos)
ClO2 = 10 (0,30 mg/l. durante 33 minutos)
Monocloramina = 100 (0,80 mg/l. durante 120 minutos)
La United States Environmental Protection Agency (USEPA) ha publicado tablascon valores de CT para inactivación de Giardia a diferentes temperaturas y pH. Así por ejemplo a la temperatura de 25ºC y pH 8,0, con un cloro residual en el rango de 1 a 2,6 mg/l, es necesario un tiempo de contacto de 54 – 65 minutos para conseguir una reducción en Giardia del 99,9 % ( 3-log.) Cuando la temperatura se reduce a 10 ºC el tiempo de contacto de eleva a 162 -194 minutos y para una temperatura de 5 ºC el tiempo de se incrementa a 304 – 368 minutos. En las tres siguientes tablas se muestran estos resultados.
Fuente: www.elaguapotable.com














Añadir comentario
Lo siento, debes estar conectado para publicar un comentario.